Investigadores de UCSD encuentran ‘portal’ que permite la infección por COVID – NBC7 San Diego
Un equipo de investigación de la Universidad de California en San Diego descubrió cómo una molécula en el exterior de la proteína espinosa SARS-Cov-2 actúa como una «puerta de entrada» al virus que causa la infección por COVID-19, lo que puede ayudar a encontrar una manera para contrarrestar el virus; Un nuevo estudio dice que todo lo que necesitamos es una ‘llave’ para bloquearlo.
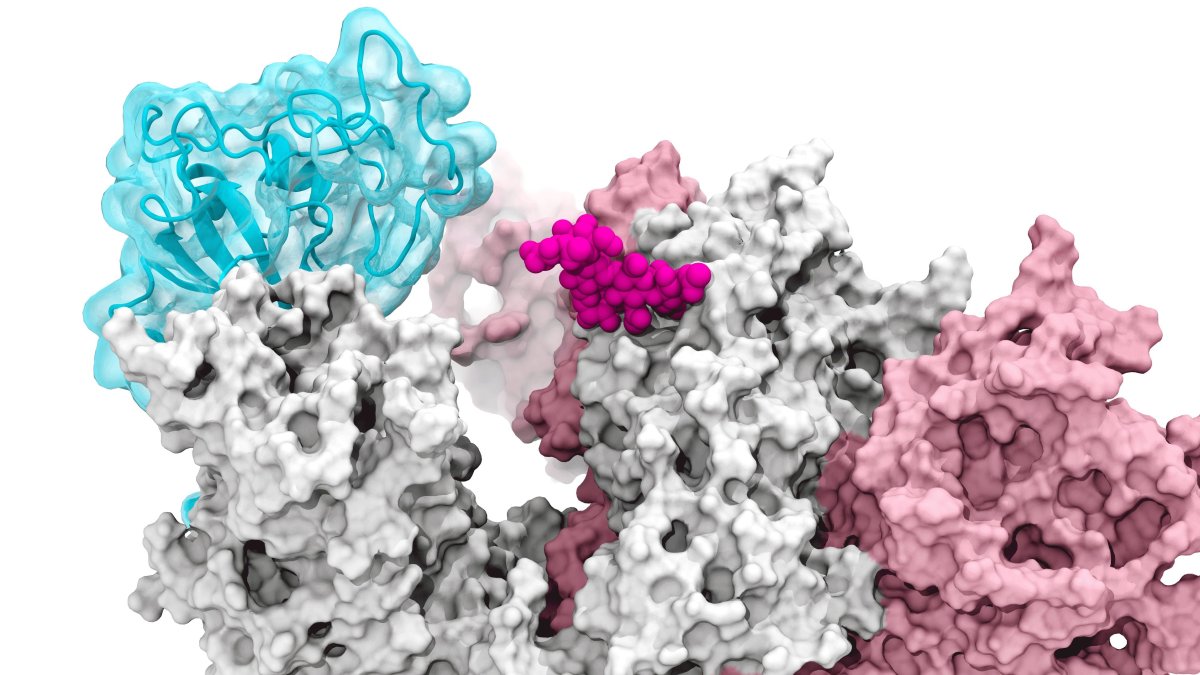
La investigación, publicada el jueves en la revista Nature Chemistry, describió cómo los glucanos, moléculas que forman un residuo glucémico alrededor de los bordes de una proteína de pico, pueden permitir que un virus ingrese e infecte células humanas sanas.
«Básicamente, descubrimos cómo se abre e infecta el pico», dijo Romi Amaro, de la Universidad de California, San Francisco, un químico físico-computacional que ayudó a desarrollar una visualización detallada de la proteína del pico del SARS-CoV-2 que se une de manera eficiente a receptores celulares.
«Hemos descubierto un secreto importante sobre el aumento repentino en la forma en que se infectan las células», dijo Amaru, profesor de química y bioquímica y uno de los autores principales del nuevo estudio. «Sin esta puerta de enlace, el virus es esencialmente incapaz de infección.»
Amaru dijo que cree que el descubrimiento del portal del equipo de investigación abre posibles vías para nuevos tratamientos para contrarrestar la infección por SARS-CoV-2. Si las compuertas de glucanos pudieran «cerrarse» farmacológicamente en la posición cerrada, se evitaría eficazmente que el virus se abriera para la entrada y la infección.
Otros participantes en el proyecto incluyen a la autora principal Lillian Chung de la Universidad de Pittsburgh, la primera autora y estudiante de posgrado de UCSF, Tera Zeten, y la co-primera autora y postdoctorado en UCSF Searle Hee Ahn.
La capa de glicanos de la espiga ayuda a engañar al sistema inmunológico humano porque no es más que un residuo azucarado, según la investigación. Las técnicas anteriores que tomaron imágenes de estas estructuras mostraban glucanos en posiciones fijas y abiertas o cerradas, lo que inicialmente no atrajo el interés de los científicos. La simulación de supercomputación permitió a los investigadores desarrollar «películas» dinámicas que revelaron que las puertas de glucanos se activaban de un sitio a otro, proporcionando una parte sin precedentes de la historia de las lesiones.

El profesor de UCSD y químico biofísico computacional Rommie Amaro, quien ayudó a desarrollar una visualización detallada de la proteína pico SARS-CoV-2 que se une de manera eficiente a nuestros receptores celulares.
“Realmente pudimos ver la apertura y el cierre”, dijo Amaru. “Esa es una de las cosas realmente interesantes que te brinda esta simulación: la capacidad de ver películas realmente detalladas.
«Cuando los miras, te das cuenta de que estás viendo algo que de otro modo hubiéramos ignorado», continuó. «Solo miras el casco cerrado, y luego miras el casco abierto, y no parece ser nada especial. Solo porque tomamos la película para todo el proceso, en realidad lo ves haciendo su trabajo».
Las simulaciones se realizaron primero en el Comet en el Centro de Supercomputación de San Diego en la Universidad de California, y más tarde en el Longhorn en la Universidad de Texas, Austin. Esta potencia informática ha proporcionado a los investigadores vistas a nivel atómico del complejo de unión al receptor de proteínas, o RBD, desde más de 300 perspectivas. Las investigaciones revelaron que el glicano ‘N343’ es la columna vertebral que mueve el RBD desde la posición ‘inferior’ a la ‘arriba’ para permitir el acceso a los receptores de la célula huésped. Los investigadores describen la activación de glucanos como algo similar al mecanismo del «disruptor molecular».

«Zombieaholic. Nerd general de Twitter. Analista. Gurú aficionado de la cultura pop. Fanático de la música».